Setelah pada bagian Identifikasi Senyawa Organik II, telah dibahas metode spektroskopi dengan ultraviolet (UV) untuk mengetahui transisi elektronik senyawaan organik, serta inframerah (IR) untuk mengetahui gugus fungsi yang terdapat dalam senyawa tersebut, kini akan disajikan metode spektroskopi lain yang turut membantu dalam elusidasi struktur senyawa organik.
Resonansi Magnetik Inti (Nuclear Magnetic Resonance; NMR)
- bahwa molekul yang dipelajari mengandung hidrogen.
- jumlah pita dalam spektrum menunjukkan bagaimana beberapa posisi yang berbeda pada molekul dimana hidrogen melekat/menempel. Frekuensi dari beberapa resonansi utama pada spektrum NMR menunjukkan perubahan kimia. Ini sangat penting untuk menduga bagian dari spektrum NMR yang mengandung informasi tentang lingkungan masing-masing atom hidrogen dan struktur dari komponen yang dipelajari.
- bahwa sebuah spektrum NMR menentukan perbandingan luas/daerah pita yang berbeda, ini menjelaskan jumlah atom hidrogen yang relatif yang keluar pada masing-masing posisi pada molekul yang diperoleh.
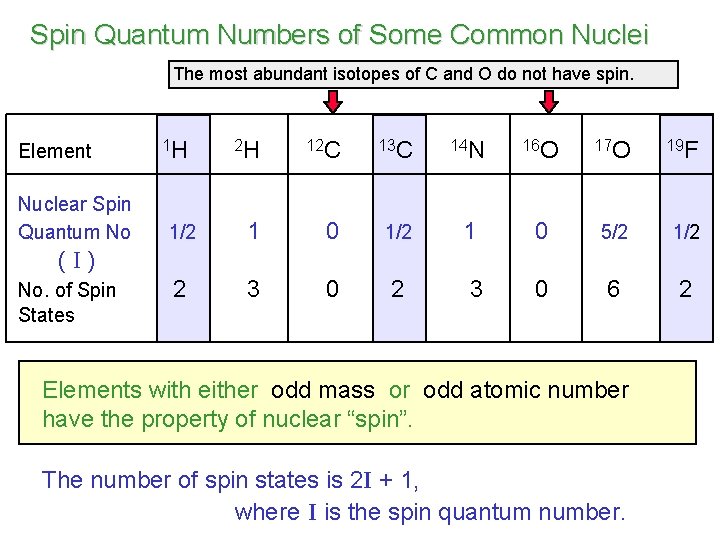
Inti-inti atom unsur-unsur dapat dikelompokkan sebagai mempunyai spin atau tidak mempunyai spin. Suatu inti berspin akan menimbulkan medan magnet kecil, yang ditunjukkan oleh suatu momen magnet nuklir, berupa suatu vektor. Diantara inti-inti yang lebih umum yang memiliki spin dan tidak memiliki spin antara lain :
Inti proton (atom hidrogen) dan karbon (karbon 13) mempunyai sifat-sifat magnet. Bila suatu senyawa mengandung hidrogen atau karbon diletakkan dalam bidang magnet yang sangat kuat dan diradiasi dengan radiasi elektromagnetik maka inti atom hidrogen dan karbon dari senyawa tersebut akan menyerap energi melalui suatu proses absorpsi yang dikenal dengan resonansi magnetik. Absorpsi radiasi terjadi bila kekuatan medan magnet sesuai dengan frekuensi radiasi elektromagnetik. Proton tunggal 1H adalah isotop yang paling penting dalam hydrogen. Isotop ini melimpah hampir 100% dan jaringan hewan mengandung 80% air. 1H memproses momen magnetik yang besar dari nuclei yang penting secara biologi. Ketika pada medan magnet konstan, frekuensi NMR dari nuclei hanya bergantung pada momen magnetnya, frekuensi 1H paling tinggi pada spekrometer yang sama. Sebagai contoh, pada spekrometer 360 MHz untuk 1H, frekuensi untuk 31P adalah 145,76 MHz dan untuk 13C adalah sekitar 90 MHz.
Dasar dari spektroskopi NMR adalah absorpsi radiasi elektromagnetik dengan frekuensi radio oleh inti atom. Frekuensi radio yang digunakan berkisar dari 0,1 sampai dengan 100 MHz. Bahkan, baru-baru ini ada spektrometer NMR yang menggunakan radio frekuensi sampai 500MHz. Skema alat NMR ditunjukkan pada gambar dibawah:
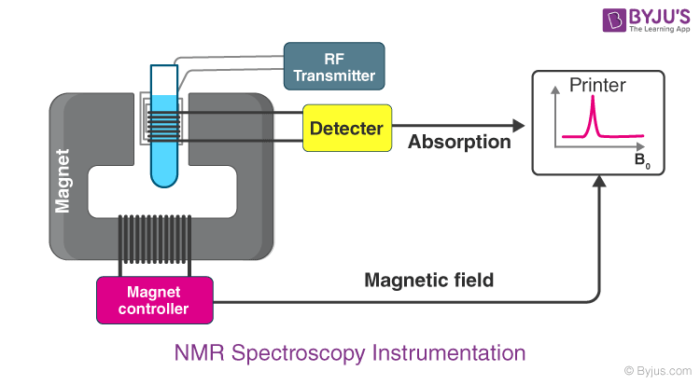 |
| Skema Alat Spektroskopi Resonansi Magnetik Inti (NMR) |
 |
| Alat NMR di Laboratorium Colorado University, USA |
Aplikasi NMR
- Bidang kedokteran
- Bidang Biologi Molekuler
- Studi Larutan NMR Pada Protein Membran
Spektrometri Massa (Mass Spectrometry; MS)
Spektometer massa adalah suatu instrumen yang dapat menyeleksi molekul-molekul gas bermuatan berdasarkan massa atau beratnya. Teknik ini tidak dapat dilakukan dengan spektroskopi, akan tetapi nama spektroskopi dipilih disebabkan persamaannya dengan pencatat fotografi dan spektrum garis optik. Umumnya spektrum massa diperoleh dengan mengubah senyawa suatu sampel menjadi ion-ion yang bergerak cepat yang dipisahkan berdasarkan perbandingan massa terhadap muatan.Proses ionisasi menghasilkan partikel-partikel bermuatan positif, dimana massa terdistribusi adalah spesifik terhadap senyawa induk. Selain untuk penentuan stuktur molekul, spektum massa dipakai untuk penentuan analisis kuantitatif. Jika didapat data IR dan NMR yang cukup lengkap, maka MS ini dapat digunakan untuk konfirmasi dengan memperhatikan bobot molekul dan kemungkinan rumus strukturnya.
Garis besar tentang apa yang terjadi dalam alat spektrometer massa ditunjukkan pada gambar berikut ini. Penjelasan mengenai cara kerja alat disampaikan pada keterangan dibawah gambar.
 |
| Skema Alat Spektrometer Massa (MS) |
- Tahap pertama : Ionisasi
- Tahap kedua : Percepatan
- Tahap ketiga : Pembelokan
- Tahap keempat : Pendeteksian
Mekanisme fragmentasi
Beberapa aturan sederhana untuk fragmentasi ion adalah sebagai berikut:




 |
| Gambar 8. Contoh mekanisme fragmentasi satu ikatan untuk ion elektron ganjil untuk memberikan ion elektron genal. Kation radikal dibuat oleh elektron dampak ionisasi seperti yang ditunjukkan pada Gambar 5. Secara umum, fragmentasi terjadi satu ikatan dihapus dari lokasi radikal kation radikal. Setiap kail ikan panah menunjukkan migrasi elektron tunggal. Ketika dua panah datang bersama-sama, ikatan baru terbentuk; ketika dua panah bergerak terpisah, sebuah ikatan terputus. Garis putus-putus menunjukkan lokasi pemutusan. |
 |
| Gambar 9. Contoh dua mekanisme fragmentasi untuk ion elektron ganjil untuk memberikan ion elektron ganjil. Kation radikal dibuat oleh elektron dampak ionisasi seperti yang ditunjukkan pada Gambar. Setiap panah menunjukkan migrasi elektron tunggal. Ketika dua panah bertemu, ikatan baru terbentuk; ketika dua panah bergerak terpisah, sebuah ikatan terputus. Garis putus-putus menunjukkan lokasi pemutusan. |
 |
| Gambar 10. Contoh mekanisme fragmentasi satu ikatan ion elektron genap diciptakan oleh ionisasi kimia dengan CH 5 + seperti yang ditunjukkan pada Gambar 6. Setiap panah melengkung menunjukkan migrasi pasangan elektron. Garis putus-putus menunjukkan ikatan yang rusak. Fragmentasi biasanya terjadi melalui hilangnya sebuah molekul kecil yang stabil seperti air. |
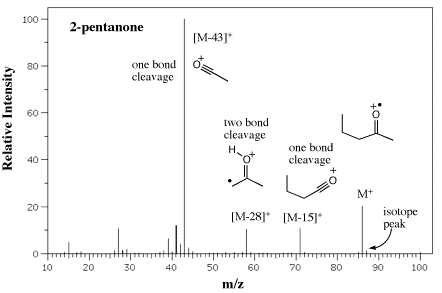 |
| Gambar 11. EI / MS dari 2-pentanone dengan penugasan beberapa satu ikatan dan dua perpecahan menggunakan mekanisme Angka 8 dan 9. |
 |
| Gambar 12. EI / MS dari N-ethylbutylamine dengan penugasan beberapa satu ikatan perpecahan menggunakan salah satu mekanisme dalam Gambar 8. |
 |
| Gambar 13. EI / MS etil butanoate (etil butirat) dengan penugasan beberapa satu dan dua ikatan perpecahan menggunakan mekanisme Angka 8 dan 9. |
- Mengetahui komposisi unsur dari bahan yang dianalisa sehingga diketahui berat dan rumus molekulnya
- Mengetahui unsure senyawa baik senyawa organic maupun anorganik
- Untuk analisis kualitatif maupun kuantitatif suatu kompleks
- Untuk penentuan struktur dari komponen permukaan padatan
- Untuk menentukan perbandingan isotop atom dalam suatu sampel
DAFTAR PUSTAKA
- Cresswell, C.J. 1982. Analisis Spektrum Senyawa Organik. Edisi kedua. Bandung: Penerbit ITB.
- Dachriyanus. 2004. Analisis Struktur Senyawa Organik secara Spektroskopi. Padang: Andalas University Press.
- Pavia, L. D. 1979. Introduction to Spectroscopy a Guide for Students of Organic Chemistry. Philladelphia: Saunders College
- Silverstein, R. M. 1986. Penyidikan Spektrometrik Senyawa Organik. Terjemahan A. J. Hatomo dan Anny Viktor Purba. Edisi ke-4. Jakarta: Penerbit Erlangga.
- Sudjadi. 1986. Metode Pemisahan. Yogyakarta: Penerbit Kanisius.
- Supratman, U. 2008. Elusidasi Struktur Senyawa Organik. Bandung: Penerbit Widya Padjadjaran.








 Time in Jakarta
Time in Jakarta 
0 comments:
Posting Komentar